Hydroxymethylace
Hydroxymethylace je chemická reakce, při které se na molekuly navazují hydroxymethylové skupiny -CH2OH. Tyto reakce mohou probíhat mnoha způsoby a mají průmyslový i biochemický význam.
Hydroxymethylace formaldehydem
K hydroxymethylacím se často používá reakce formaldehydu s aktivními vazbami C-H a N-H:
- R3C-H + CH2O → R3C-CH2OH
- R2N-H + CH2O → R2N-CH2OH
Aktivní vazbou C-H bývá koncový alkyn[1] nebo alfa proton aldehydu.[2]
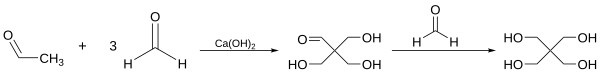
Pentaerythritol se vyrábí hydroxymethylací acetaldehydu:
S formaldehydem mohou reagovat také vazby P-H; takto se připravuje tetrakis(hydroxymethyl)fosfoniumchlorid ([P(CH2OH)4]Cl) z fosfanu (PH3).[3]
Hydroxymethylace v rámci demethylace
U 5-methylcytosinu dochází k oxidaci methylové skupiny, přičemž se předpokládá, že je tato úprava předstupněm demethylace, obnovující původní cytosin:[4]
- RCH3 + O → RCH2OH
Příklady
Při dvoukrokové hydroxymethylaci aldehydů proběhne nejprve methylenace, po které následuje hydroboračně-oxidační reakce:[5]
- RCHO + Ph3P=CH2 → RCH=CH2 + Ph3PO
- RCH=CH2 + R2BH → RCH2-CH2BR2
- RCH2-CH2BR2 + H2O2 → RCH2-CH2OH + HOBR2
Silylmethylovanými Grignardovými činidly lze hydroxymethylovat ketony:[6]
- R2C=O + ClMgCH2SiR'3 → R2C(OMgCl)CH2SiR'3
- R2C(OMgCl)CH2SiR'3 + H2O + H2O2 → R2C(OH)CH2OH + HOSiR'3
Reakce hydroxymethylovaných sloučenin
Hydroxymethylované sloučeniny často reagují s druhým ekvivalentem aktivní vazby X-H:
- hydroxymethylace: X-H + CH2O → X-CH2OH
- překřížení: X-H + X-CH2OH → X-CH2-X + H2O
Tato reaktivita se využívá při výrobě polymerů a pryskyřic (bakelitu, novolaku, a kalixarenů) kondenzacemi formaldehydu s fenoly; podobně může formaldehyd kondenzovat také s močovinou.
Hydroxymethylace vazeb N-H a P-H lze často obrátit přidáním zásady; příkladem může být příprava tris(hydroxymethyl)fosfinu:[7]
- [P(CH2OH)4]Cl + NaOH → P(CH2OH)3 + H2O + H2C=O + NaCl
Za přítomnosti chloračních činidel místo hydroxymethylací probíhají chlormethylace, například Blancova chlormethylace.
Podobné reakce
- Při hydroxyethylacích se navazují skupiny -CH2CH2OH; tyto reakce se využívají jako součásti ethoxylací.
- Aminomethylace se často provádějí pomocí Eschenmoserovy soli, [(CH3)2NCH2]OTf.[8]
Reference
V tomto článku byl použit překlad textu z článku Hydroxymethylation na anglické Wikipedii.
- ↑ John Hooz; Jorge Cabezas; Sergio Musmanni; Jose Calzada. Propargylation of Alkyl Halides: (E)-6,10-Dimethyl-5,9-Undecadien-1-Yne and (E)-7,11-Dimethyl-6,10-Dodecadien-2-yn-1-ol. Organic Syntheses. 1990, s. 120. Dostupné online. doi:10.15227/orgsyn.069.0120.
- ↑ Robert K. Boeckman; Douglas J. Tusch; Kyle F. Biegasiewicz. Organocatalyzed Direct Asymmetric α-Hydroxymethylation of Aldehydes. Organic Syntheses. 2015, s. 320-327. doi:10.15227/orgsyn.092.0320.
- ↑ Ullmann's Encyclopedia of Industrial Chemistry. Příprava vydání Wiley-VCH. 1. vyd. [s.l.]: Wiley Dostupné online. ISBN 978-3-527-30385-4, ISBN 978-3-527-30673-2. doi:10.1002/14356007.a19_545.pub2. (anglicky) DOI: 10.1002/14356007.
- ↑ Carolina M. Greco, Paolo Kunderfranco, Marcello Rubino, Veronica Larcher, Pierluigi Carullo, Achille Anselmo, Kerstin Kurz, Thomas Carell, Andrea Angius, Michael V. G. Latronico, Roberto Papait, Gianluigi Condorelli. DNA hydroxymethylation controls cardiomyocyte gene expression in development and hypertrophy. Nature Communications. 2016, s. 12418. doi:10.1038/ncomms12418. PMID 27489048. Bibcode 2016NatCo...712418G.
- ↑ Eric J. Leopold. Selective Hydroboration of a 1,3,7-Triene: Homogeraniol. Organic Syntheses. 1986, s. 164. doi:10.15227/orgsyn.064.0164.
- ↑ Kohei Tamao; Neyoshi Ishida; Yoshihiko Ito; Makoto Kumada. Nucleophilic Hydroxymethylation by the (Isopropoxydimethylsilyl)Methyl Grignard Reagent: 1-(Hydroxymethyl)Cyclohexanol from Cyclohexanone. Organic Syntheses. 1990, s. 96. doi:10.15227/orgsyn.069.0096.
- ↑ M. Caporali; L. Gonsalvi; F. Zanobini; M. Peruzzini. Synthesis of the Water-Soluble Bidentate (P,N) Ligand PTN(Me). Inorganic Syntheses. 2011, s. 92-108. doi:10.1002/9780470651568.ch5.
- ↑ Michel Gaudry; Yves Jasor; Trung Bui Khac. Regioselective Mannich Condensation with Dimethyl(Methylene)Ammonium Trifluoroacetate: 1-(Dimethylamino)-4-Methyl-3-Pentanone. Organic Syntheses. 1979, s. 153. doi:10.15227/orgsyn.059.0153.